9月2日,我校检验医学院、临床检验诊断学教育部重点实验室柳满然教授团队在国际学术期刊《Cancer Communications》发表题为“Tryptophan 2,3-dioxygenase-positive matrix fibroblasts fuel breast cancer lung metastasis via kynurenine-mediated ferroptosis resistance of metastatic cells and T cell dysfunction”的研究论文。

肿瘤转移是导致癌症相关死亡的主要原因。许多实体肿瘤的远处器官转移表现出非随机分布,这一现象被称为“肿瘤的嗜器官转移”。肺是乳腺癌最常见的转移部位之一,但关于肿瘤细胞对远处器官选择的认识仍然不足。器官特异性生态位在肿瘤的嗜器官转移中起关键作用。作为转移微环境中重要的组成部分,转移相关成纤维细胞(MAFs)及其异质性如何影响转移灶形成尚不清楚。
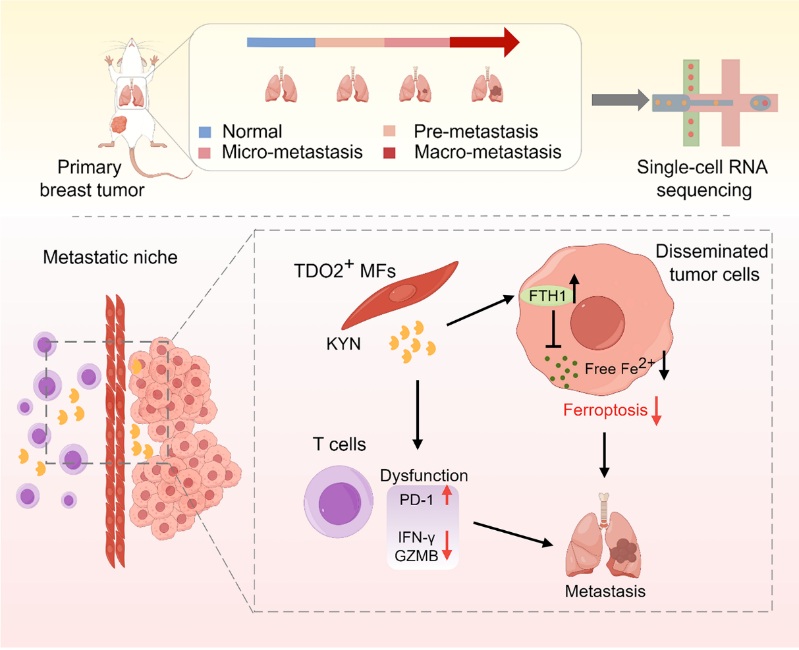
该研究利用小鼠乳腺癌嗜肺转移模型,借助单细胞测序,揭示了特定成纤维细胞亚群在促进播散肿瘤细胞(DTCs)肺转移和免疫逃逸中的重要作用。研究结果显示,转移灶中激活的成纤维细胞亚群MFs存在异常的色氨酸2,3-双加氧酶(TDO2)高表达,从而导致大量犬尿氨酸(KYN)的分泌。TDO2-KYN轴显著提高DTCs中铁蛋白重链1(FTH1)的表达,进而降低DTCs细胞质中游离Fe2+水平,增强DTCs对铁死亡的抵抗力;同时,TDO2+MFs分泌的趋化因子CCL8和CCL11募集T细胞,而TDO2+MFs来源的KYN诱导T细胞功能障碍,支持DTCs的免疫逃逸。
该研究在单细胞水平揭示了DTCs、T细胞和TDO2+MFs之间的特异性互作,这不仅为乳腺癌肺转移机制提供了新的、有价值的认知,并为开发针对转移性疾病的未来治疗提供有用的靶点。
我校检验医学院柳满然教授为本文通讯作者,研究生刘永灿和陈善春为第一作者,该研究同时得到了海外学者崔晓江教授和滕勇教授的大力协助,并获得科技部国家重点计划项目、国家自然科学基金、校拔尖人才特聘教授项目、重庆市高校创新项目等基金的资助。
原文链接:https://pubmed.ncbi.nlm.nih.gov/39221971/















