近日,欧洲分子生物学学会期刊《The EMBO Journal》编辑部传来喜报,我校杨帆博士、李晶晶博士和邓海君博士作为共同第一作者在线发表了题为“GSTZ1-1 Deficiency Activates NRF2/IGF1R Axis in HCC via Accumulation of Oncometabolite Succinylacetone”的论文(DOI 10.15252/embj.2019101964,影响因子11.227),汪凯博士、唐霓教授和黄爱龙教授系该论文共同通讯作者。该论文通过组学数据分析、质谱鉴定和实验验证,首次完整地阐述了肝癌中GSTZ1缺失导致NRF2/IGF1R信号轴激活的分子机理。与此同时,作者提出了琥珀酰丙酮是一种新的致癌代谢物,其通过修饰KEAP1蛋白406位半胱氨酸上的巯基,激活NRF2/IGF1R信号轴,促进肝癌发生发展的新机制。上述研究首次鉴定了琥珀酰丙酮对KEAP1蛋白的翻译后修饰,进一步加深了对苯丙氨酸/酪氨酸代谢异常在肝癌发生发展中的认识。
通过前期生物信息学分析,课题组发现肝癌组织中多个代谢基因表达量显著低于正常肝组织,其中包括GSTZ1基因编码的谷胱甘肽S-转移酶ζ1,是负责催化苯丙氨酸/酪氨酸分解代谢倒数第二步反应的关键酶,也称为马来酰乙酰乙酸异构酶。该代谢通路中多种酶的突变与代谢性疾病有关,包括尿黑酸症、苯丙酮尿症和酪氨酸血症等。其中I型酪氨酸血症由该通路倒数第一步反应的延胡索酰乙酰乙酸水解酶(FAH)突变引起,可导致肝硬化和肝癌的发生。而GSTZ1的异常低表达是否也参与肝癌的发生发展却鲜有报道。
课题组首先建立了GSTZ1基因敲除和过表达肝癌细胞模型、裸鼠皮下移植瘤模型、以及DEN诱导的GSTZ1基因敲除小鼠肝癌模型,证实了GSTZ1在肝癌中发挥抑癌基因的功能,回复GSTZ1基因表达能够抑制肝癌细胞增殖和克隆形成。然后通过质谱分析,检测到GSTZ1基因缺失小鼠肝脏组织中苯丙氨酸/酪氨酸分解代谢产物琥珀酰丙酮堆积,并发现琥珀酰丙酮可以修饰KEAP1蛋白406位半胱氨酸上的巯基,从而激活NRF2,促进其核转位。NRF2与SP1转录因子相互作用,促进后者与胰岛素样生长因子受体1(IGF1R)启动子结合,上调IGF1R的表达,从而激活下游的抗凋亡信号通路。进一步研究发现,NRF2抑制剂鸦胆子苦醇(Brusatol)及IGF1R抑制剂鬼臼苦素(Picropodophyllin)可以促进肝癌细胞的凋亡,抑制GSTZ1基因敲除小鼠肝癌的生长和肿瘤结节形成。
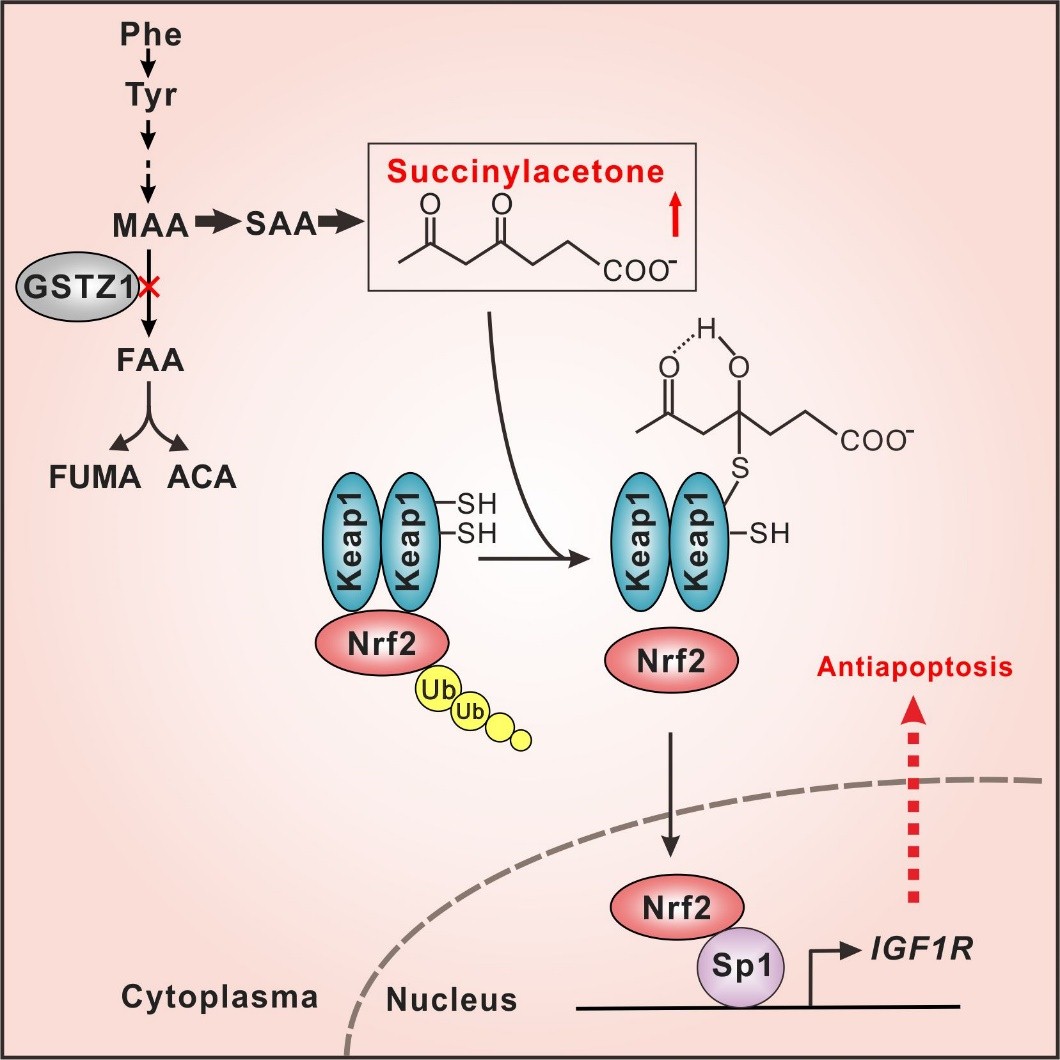
细胞稳态主要由细胞代谢与信号转导途径共同维持。近年来研究发现,一些内源性代谢物可以与蛋白质形成功能性的共价修饰,参与细胞功能的调节。例如糖代谢过程中的代谢物富马酸(延胡索酸)、衣康酸和丙酮醛等,可选择性地修饰KEAP1蛋白上的半胱氨酸残基,并激活NRF2信号通路。本研究首次发现苯丙氨酸/酪氨酸分解代谢产物琥珀酰丙酮可以修饰KEAP1蛋白上的406位半胱氨酸残基,从而激活NRF2。而NTBC [2-(2-硝基-4-三氟甲基苯甲酰基)-环己烷-1,3-二酮]能够抑制苯丙氨酸/酪氨酸分解代谢通路中4-对羟基苯丙酮酸双氧化酶(4-HPPD)的活性,从而阻断该代谢通路异常造成的促肿瘤效应。这一发现不仅证实了KEAP1的406位半胱氨酸残基能够感知细胞内源代谢物,参与NRF2/IGF1R信号轴的调控,还为肝癌中IGF1R信号通路的过度活化提供了新的见解,并提出了潜在的治疗策略。
琥珀酰丙酮烷基化修饰KEAP1蛋白的鉴定工作,得到了合作单位军事医学研究院生命组学研究所徐平研究员团队的帮助。该成果由国家自然科学基金(81872270,81661148057,81602417)、国家科技重大专项(2017ZX10202203)、重庆市科技创新领军人才计划、重庆市高校创新团队等项目资助。















